Что такое коррозийная стойкость
Способность того или иного металла сопротивляться коррозии, называется коррозийной стойкостью. Эта способность определяется скоростью протекания коррозии в определенных условиях. Чтобы оценить скорость коррозии, используют количественные и качественные характеристики.

Качественные характеристики — это:
-
изменение внешнего вида поверхности металла;
-
изменение микроструктуры металла.
Количественные характеристики — это:
-
время до появления первого очага коррозии;
-
количество очагов коррозии, образовавшихся за некоторый промежуток времени;
-
утончение металла за единицу времени;
-
изменение массы металла на единицу площади поверхности за единицу времени;
-
объем поглощенного или выделившегося газа в процессе коррозии на единице поверхности за единицу времени;
-
плотность электрического тока для данной скорости коррозии;
-
изменение того или иного свойства за определенный промежуток времени (механические свойства, отражательная способность, электрическое сопротивление).
Для разных металлов характерна разная стойкость к коррозии. Чтобы устойчивость к коррозии повысить, используют специальные методы: легирование для стали, хромирование, алитирование, никелирование, окраска, цинкование, пассивация и т.д.
Железо и сталь

В присутствии кислорода и чистой воды, железо быстро корродирует, реакция идет по формуле:
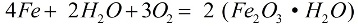
В процессе коррозии, рыхлый слой ржавчины покрывает металл, и этот слой отнюдь не защищает его от дальнейшего разрушения, коррозия идет до полного уничтожения металла. Более активную коррозию железа вызывают растворы солей: если в воздухе присутствует даже немного хлорида аммония (NH4Cl), коррозийный процесс пойдет значительно быстрее. В слабом растворе соляной кислоты (HСl) реакция тоже активно пойдет.
Азотная кислота (HNO3) в концентрации более 50% вызовет пассивацию металла, - он покроется хоть и хрупким, но все же защитным слоем. Дымящая азотная кислота безопасна для железа.
Серная кислота (H2SO4) в концентрации более 70% пассивирует железо, а если сталь марки Ст3 держать в 90% серной кислоте при температуре 40°С, то в данных условиях скорость ее коррозии не превысит 140 мкм в год. Если же температура составит 90°С, то коррозия пойдет с в 10 раз большей скоростью. Серная кислота концентрацией 50% железо растворит.
Ортофосфорная кислота (H3PO4) не вызовет коррозии железа, как и безводные органические растворители, как растворы щелочей, водный аммиак, сухие Вr2 и Сl2.
Если к воде добавить тысячную долю хромовокислого натрия, то он станет отличным ингибитором коррозии железа, как и натрия гексаметафосфат. А вот ионы хлора (Cl-) снимают с железа защитную пленку и усиливают коррозию. Железо технически чистое, в котором содержится примерно 0,16% примесей, отличается высокой устойчивости к коррозии.
Стали среднелегированные и низколегированные
Легирующие добавки хрома, никеля или меди в низколегированных и среднелегированных сталях повышают их устойчивость к водной и атмосферной коррозии. Чем больше хрома — тем выше устойчивость стали к окислению. Но если хрома меньше 12%, то химически активные среды подействуют на такую сталь разрушительно.
Высоколегированные стали
В высоколегированных сталях легирующих компонентов больше 10%. Если в стали содержится от 12 до 18% хрома, то такая сталь выдержит контакт почти с любой из органических кислот, с пищевыми продуктами, окажется стойкой к азотной кислоте (HNO3), к щелочам, ко многим растворам солей. В 25% муравьиной кислоте (CH2O2) коррозия высоколегированной стали пойдет со скоростью порядка 2 мм в год. Однако сильные восстановители, соляная кислота, хлориды и галогены разрушат высоколегированную сталь.
Стали нержавеющие, в которых содержится от 8 до 11% никеля и от 17 до 19% хрома более стойки к коррозии чем просто высокохромистые стали. Такие стали выдерживают кислые окислительные среды, как то хромовокислая или азотокислая, а также сильные щелочные.
Никель в качестве добавки усилит стойкость стали к неокислительным средам, к атмосферным факторам. Но среды кислые восстановительные и кислые с ионами галогенов, - разрушат пассивирующий оксидный слой, в результате сталь потеряет устойчивость к кислотам.
Более высокую коррозийную устойчивость, чем хромоникелевые стали, имеют стали нержавеющие с добавлением молибдена в количестве от 1 до 4%. Молибден даст стойкость к сернистой и серной кислотам, к органическим кислотам, к морской воде и галогенидам.
Ферросилиций (железо с добавлением от 13 до 17% кремния), так называемое железокремнистое литье, обладает коррозийной стойкостью благодаря наличию оксидной пленки SiO2, и которую не способны разрушить ни серная, ни азотная, ни хромовая кислоты, они лишь усиливают эту защитную пленку. А вот соляная кислота (HCl) легко приведет к коррозии ферросилиция.
Сплавы никеля и чистый никель

Никель стоек ко многим факторам, как к атмосферным, так и к лабораторным, к чистой и соленой воде, к щелочным и нейтральным солям, таким как карбонаты, ацетаты, хлориды, нитраты и сульфаты. Не насыщенные кислородом и не горячие органические кислоты не причинят вреда никелю, как и кипящая концентрированная щелочь гидроксид калия (KOH) в концентрации до 60%.
Коррозию вызовут восстановительные и окислительные среды, окислительные щелочные или кислые соли, окислительные кислоты, такие как азотная, влажные газообразные галогены, оксиды азота и диоксид серы.
Монель-металл (до 67 % никеля и до 38 % меди) более стоек к действию кислот, чем чистый никель, но действие сильных окисляющих кислот не выдержит. Отличается довольно высокой стойкостью к кислотам органическим, к значительному количеству растворов солей. Атмосферная и водная коррозия не грозят монель-металлу, безопасен для него также фтор. Монель-металл безопасно выдержит действие кипящего фтороводорода (HF) концентрацией 40%, как его выдерживает платина.
Сплавы алюминия и чистый алюминий

Защитная оксидная пленка алюминия делает его устойчивым к обычным окислителям, к уксусной кислоте, к фтору, просто к атмосфере, и к значительному количеству органических жидкостей. Технически чистый алюминий, в котором примесей меньше 0,5%, очень стоек к действию перекиси водорода (H2O2).
Разрушается под действием едких щелочей сильных восстановительных сред. Разбавленная серная кислота и олеум не страшны алюминию, но серная кислота средней концентрации его разрушит, как и горячая азотная кислота.
Защитную оксидную пленку алюминия способна разрушить соляная кислота. Контакт алюминия со ртутью или с солями ртути разрушителен для первого.
Чистый алюминий более устойчив к коррозии, чем например сплав дюралюминий (в котором до 5,5% меди, 0,5% магния и до 1% марганца), который менее стоек к коррозии. Силумин (добавка от 11 до 14% кремния) в этом отношении более устойчив.
Сплавы меди и чистая медь

Чистая медь и ее сплавы не корродируют ни в соленой воде, ни на воздухе. Не страшны меди в плане коррозии: разбавленные щелочи, сухой NH3, нейтральные соли, сухие газы и большинство органических растворителей.
Такие сплавы как бронза, в которых содержится много меди, выдерживают нахождение в кислотах, даже в холодной концентрированной или в горячей разбавленной серной кислоте, либо в концентрированной или разбавленной соляной кислоте при обычной температуре (25°С).
В отсутствие кислорода медь не корродирует при контакте с органическими кислотами. Не оказывают разрушительного действия на медь ни фтор, ни сухой фтороводород.
Но медные сплавы и чистая медь корродируют от различных кислот если есть кислород, а также при контакте с влажным NH3, некоторыми кислыми солями, влажными газами, типа ацетилена, CO2, Cl2, SO2. Медь легко взаимодействует со ртутью. Латунь (цинк и медь) не отличается высокой устойчивостью к коррозии.
Подробнее смотрите здесь - Медь и алюминий в электротехнике
Чистый цинк

Чистая вода, ровно как и чистый воздух, не приводит к коррозии цинка. Но если в воде или в воздухе присутствуют соли, углекислый газ или аммиак, то начнется коррозия цинка. Цинк растворяется в щелочах, особенно быстро — в азотной кислоте (HNO3), медленнее — в соляной и серной кислотах.
Органические растворители и нефтепродукты в принципе не оказывают корродирующего действия на цинк, но если контакт будет длительным, с крекинг-бензином, например, то кислотность бензина повысится при окислении его на воздухе, и начнется коррозия цинка.
Чистый свинец

Высокая устойчивость свинца к водной и атмосферной коррозии — известный факт. Не корродирует свинец и при нахождении в почве. Но если в воде содержится много углекислого газа, то свинец в ней растворится, поскольку образуется гидрокарбонат свинца, который уже будет растворим.
В целом свинец очень стоек к растворам нейтральным, умеренно стоек к щелочным, а также к некоторым кислотам: серной, фосфорной, хромовой и сернистой. Концентрированной серной кислотой (от 98%) при температуре в 25°С, свинец можно медленно растворить.
Фтороводород при концентрации 48% растворит свинец при нагревании. Сильно взаимодействует свинец с соляной и азотной кислотами, с муравьиной и уксусной кислотой. Серная кислота покроет свинец труднорастворимым слоем хлорида свинца (PbCl2), и дальше растворение уже не пойдет. В концентрированной азотной кислоте свинец также покроется слоем соли, но разбавленная азотная кислота растворит свинец. Хлориды, карбонаты и сульфаты к свинцу не агрессивны, а растворы нитратов — наоборот.
Чистый титан

Хорошая коррозийная устойчивость — отличительная черта титана. Он не окисляется сильными окислителями, выдерживает растворы солей, FeCl3 и т.д. Концентрированные минеральные кислоты вызовут коррозию, однако даже кипящая азотная кислота в концентрации менее 65%, серная — до 5%, соляная — до 5% - коррозии титана не вызовут. Нормальная коррозийная устойчивость к щелочам, к щелочным солям и органическим кислотам выделяет титан в ряду других металлов.
Чистый цирконий

Цирконий более устойчив к серной и соляной кислотам чем титан, однако к царской водке и влажному хлору — устойчив менее. Обладает высокой химической стойкостью к большинству щелочей и кислот, устойчив к перекиси водорода (H2O2).
Действие некоторых хлоридов, кипящая концентрированная соляная кислота, царская водка (смесь концентрированных азотной HNO3 (65—68 % масс.) и соляной HCl (32—35 % масс.), горячая концентрированная серная кислота и дымящая азотная — вызывают коррозию. Очень значимым в плане коррозии является такое свойство циркония, как гидрофобность, то есть этот металл не смачивается ни водой, ни водными растворами.
Чистый тантал

Превосходная химическая стойкость тантала подобна стеклу. Его плотная оксидная пленка защищает металл при температурах до 150°С от действия хлора, брома, йода. Большинство кислот в нормальных условиях не действуют на тантал, даже царская водка и концентрированная азотная кислота не вызывают коррозии. Растворы щелочей практически не действуют на тантал, но на него действуют фтороводород и концентрированные горячие растворы щелочей, чтобы растворить тантал, применяют расплавы щелочей.