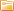Вещества, в которых электрический ток обусловлен движением ионов, то есть ионной проводимостью, называются электролитами. Электролиты относятся к проводникам второго рода, поскольку ток в них связан с химическими процессами, а не просто с движением электронов, как например в металлах.
Молекулы данных веществ в растворе способны к электролитической диссоциации, то есть они распадаются при растворении на положительно заряженные (катионы) и отрицательно заряженные (анионы) ионы. В природе можно встретить твердые электролиты, ионные расплавы и растворы электролитов. В зависимости от вида растворителя, электролиты бывают водные и неводные, а также особый вид - полиэлектролиты.
В зависимости от вида ионов, на которые распадается вещество при растворении в воде, можно выделить электролиты без ионов Н+ и ОН- (солевые электролиты), электролиты с обилием ионов Н+ (кислоты) и электролиты с преобладанием ионов ОН- (основания).
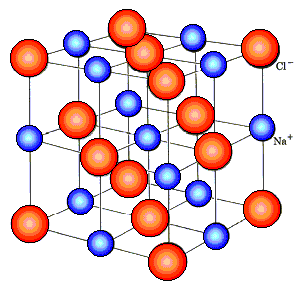
Если при диссоциации молекул электролита образуется равное число положительных и отрицательных ионов, такой электролит называется симметричным. Или же несимметричным, если количество положительных и отрицательных ионов в растворе не одинаково. Примеры симметричных электролитов — KCL-1,1-валентный электролит и CaSO4 – 2,2-валентный электролит. Представителем несимметричного электролита является, например, H2SO4 – 1,2-валентный электролит.

Все электролиты можно условно разделить на сильные и слабые, в зависимости от их способности к диссоциации. Сильные электролиты в разбавленных растворах почти полностью распадаются на ионы. К ним относится большое количество неорганических солей, некоторые кислоты и основания в водных растворах или растворителях с высокой диссоциирующей способностью, таких как спирты, кетоны или амиды.
Слабые электролиты распадаются лишь частично, и пребывают в динамическом равновесии с недиссоциированными молекулами. К ним относится большое количество органических кислот, а также многие основания в растворителях.
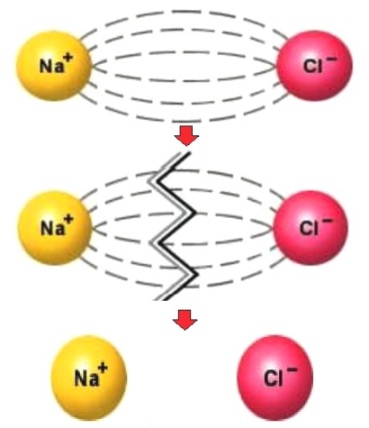
Степень диссоциации зависит от нескольких факторов: от температуры, от концентрации, от вида растворителя. Так, один и тот же электролит при разной температуре или при одинаковой температуре, но в разных растворителях, будет диссоциирован в разной степени.
Поскольку электролитическая диссоциация по определению порождает большее количество частиц в растворе, это приводит к значительным различиям в физических свойствах растворов электролитов и веществ иного рода: увеличивается осмотическое давление, изменяется температура замерзания по отношению к чистому растворителю и т. д.
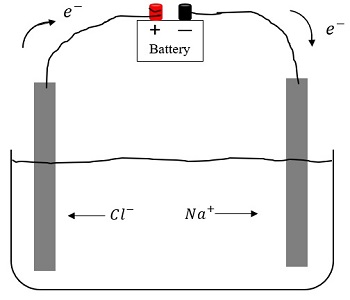
Часто ионы электролита участвуют в электрохимических процессах и химических реакциях как самостоятельные кинетические единицы, независимо от других присутствующих в растворе ионов: на электродах, погруженных в электролит, при прохождении через электролит тока, протекают окислительно-восстановительные реакции, продукты которых добавляются в состав электролита.
Таким образом, электролиты — это сложные системы веществ, включающие в себя ионы, молекулы растворителя, недиссоциированные молекулы растворенного вещества, ионные пары и более крупные соединения. И свойства электролитов определяются поэтому целым рядом факторов: характером ион-молекулярных и ион-ионных взаимодействий, изменением структуры растворителя при наличии растворенных частиц и т. д.
Ионы и молекулы полярных электролитов очень активно взаимодействуют друг с другом, что приводит к формированию сольватных структур, роль которых становится значительнее с уменьшением размеров ионов и с ростом их валентностей. Энергия сольватации является мерой взаимодействия ионов электролита с молекулами растворителя.
Электролиты, в зависимости от их концентрации, бывают: разбавленными растворами, переходными и концентрированными. Разбавленные растворы близки по структуре к чистому растворителю, но присутствующие ионы нарушают эту структуру своим влиянием. Такие слабые растворы сильных электролитов отличаются от идеальных растворов по свойствам в силу электростатического взаимодействия между ионами.
Переходная область концентрации характеризуется значительным изменением структуры растворителя из-за влияния ионов. При еще более высокой концентрации большинство молекул растворителя участвуют в сольватационных структурах с ионами, создавая таким образом дефицит растворителя.
Концентрированный же раствор имеет структуру близкую к ионному расплаву или кристаллосольвату, отличающуюся высокой упорядоченностью и единообразием ионных структур. Такие ионные структуры связываются друг с другом и с молекулами воды в ходе сложных взаимодействий.
Для электролитов характерны высокотемпературная и низкотемпературная области их свойств, а также области высоких и нормальных давлений. С ростом давления или температуры снижается молярная упорядоченность растворителя, слабеет влияние ассоциативных и сольватационных эффектов на свойства раствора. А когда температура падает ниже температуры плавления — некоторые электролиты переходят в стеклообразное состояние. Примером такого электролита может служить водный раствор LiCl.
Сегодня электролиты играют особую важную роль в мире техники и биологии. В биологических процессах электролиты выступают средой неорганического и органического синтеза, а в технике — основой электрохимических производств.
Электролиз, электрокатализ, коррозия металлов, электрокристаллизация — данные явления занимают важные места во многих современных производствах, особенно применительно к энергетике и защите окружающей среды.
Смотрите также: Получение водорода электролизом воды - технология и оборудование